 Imagerie fonctionnelle :
Imagerie fonctionnelle :
Théranostic, vous connaissez ?
Après avoir exploré des modalités d’imagerie essentiellement anatomiques, comme l’interventionnel et la mammographie, conçues et produites à Buc, ou d’autres comme l’IRM et le scanner conçues dans d’autres pôles de la société, tournons-nous aujourd’hui vers l’imagerie fonctionnelle, et en particulier vers un nouveau domaine associant Imagerie et Thérapie : le théranostic.
Pour réaliser le théranostic, nul besoin de choisir entre TEMP (tomographie par émission monophotonique permettant de réaliser une scintigraphie) et TEP (tomographie par émission de positrons) : toutes deux peuvent être utilisées pour le théranostic. Cela signifie que le théranostic peut aussi bien être réalisé sur une gamma-caméra utilisée habituellement pour produire des scintigraphies, ou sur un TEP (utilisé essentiellement pour la détection et le suivi du cancer).
Théranostic : le retour
Or, et ce n’est pas nouveau, de nombreux chercheurs ont vu dans le principe de fonctionnement de la TEMP et de la TEP, une occasion d’associer plus étroitement imagerie et traitement.
Nous avons posé la question à notre collègue, Sarah Roy, Chef des Applications Cliniques de l’Imagerie Fonctionnelle, à l’échelon européen, au sein de GE Healthcare.
Quelles nouveautés en imagerie fonctionnelle ? Vois-tu des avancées au niveau technologique ?
« Tout d’abord, je simplifierai la présentation de la médecine nucléaire pour qu’enfin tout le monde comprenne. La réelle différence entre TEMP et TEP c'est le traceur : l'un est émetteur gamma (TEMP), l'autre beta+ (TEP). Sur une gamma-caméra pour faire du TEP, il faut juste injecter un émetteur beta au patient, enlever les collimateurs, et avoir un cristal épais qui permet de faire aussi bien du TEMP que du TEP.
En ce moment, l’imagerie fonctionnelle est en plein dans le « théranostic ». En réalité c’est « vieux comme Hérode », mais les nouvelles molécules en particulier pour le cancer de la prostate sont porteuses. Elles permettent, comme l’I131 pour la thyroïde, de faire une image et de traiter en même temps.GE axe son discours sur ces nouveautés, plus que sur les systèmes, car ce sont en général les molécules qui représentent les avancées.
Et, dans cette situation, la TEMP (la tomographie par émission monophotonique) est aussi importante que la TEP (la tomographie par émission de positrons) pour le théranostic, car la molécule qui traite est émetteur gamma, donc non seulement elle traite, mais on peut faire une image TEMP grâce à cette molécule.Le théranostic, également appelé thérapie radionucléide ciblée ou radiothérapie interne vectorisée, est la combinaison de deux mots, thérapeutique (= traitement) et diagnostic (= trouver quelque chose). Pour trouver l’origine de la tumeur et traiter le patient, la même molécule est utilisée. Même si la molécule utilisée est la même pour le traitement et pour le diagnostic, les doses injectées varient, et le radionucléide peut être différent.
Pour le suivi du cancer prostatique, on dispose d’un marqueur spécifique, le PSMA (prostate-specific membrane antigen), reflétant le développement du cancer de la prostate. Marqué au gallium (Ga PSMA), on obtient ainsi un nouveau radiotraceur qui cible cet antigène membranaire spécifique (PSMA) pour l’imagerie TEP du cancer de la prostate. Une fois l'imagerie TEP réalisée, on décidera alors de traiter ou non le patient.
Le traitement s'effectuera avec du Lu PSMA. Le Lu sera à la fois émetteur bêta-moins, ce qui tuera la cellule cancéreuse, et émetteur gamma ce qui permettra de faire l'imagerie TEMP pour le suivi du traitement. Il peut délivrer des radiations directement aux cellules cancéreuses, détruisant ainsi les cellules ciblées.
Cette radiothérapie ciblée, connue sous le nom de radioligandie, fait actuellement l’objet d’essais cliniques pour son innocuité et son efficacité dans le traitement du cancer de la prostate. »
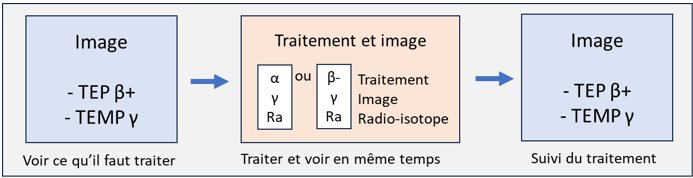
Schéma de principe du théranostic :
Une 1ère image est réalisée en TEP ou en TEMP. Le traitement s’opère ensuite grâce aux émetteurs α (alpha) ou β (bêta) qui libèrent leur énergie à proximité des cellules cibles, et tuent la tumeur et le gamma pour l’image TEMP, puis suivi du résultat en TEP ou en TEMP.
L’action biologique d’un radiopharmaceutique dépend du type de rayonnements ionisants émis par le radionucléide. Les radionucléides qui conviennent le mieux pour le traitement des tumeurs émettent des rayonnements ionisants ayant un faible pouvoir de pénétration dans les tissus, comme les émetteurs α (alpha) ou β (bêta), qui libèrent leur énergie à proximité de leurs cibles.
Premières évaluations
« Alors que nous continuons à voir de nouveaux traceurs et thérapies approuvés par la FDA arriver sur le marché, nous sommes enthousiasmés par de nouvelles opportunités d’adopter la théranostique dans la pratique clinique quotidienne.
Ceci permet des soins plus personnalisés aux patients pour de meilleurs résultats ». Cela a été déclaré par le Dr Anthony Chang, fondateur et PDG de BAMF (Bold Advanced Medical Future) Health, situé à Grand Rapids dans l’état du Michigan aux Etats-Unis.
« La radiothérapie PSMA pour le cancer de la prostate est le traitement le plus récemment approuvé, mais il existe une grande opportunité pour l’application de la théranostique à diverses formes de cancer. Nous voyons aujourd’hui d’excellentes opportunités avec nos systèmes PETtrace et StarGuide. Nous attendons donc avec impatience une adoption plus large de la théranostique pour réaliser ce que nous avons appelé une véritable « médecine de précision basée sur l’intelligence », le tout en une seule session. »
L’avancement des technologies d’imagerie, l’évolution et la découverte compte tenu des nouveaux traceurs et thérapies ciblées, inaugure une nouvelle ère dans les soins de santé. Une ère dans laquelle la santé de précision, et la théranostique, sont au cœur de leurs préoccupations. Le cancer de la prostate n’est qu’un début, avec de nombreuses autres applications en cours de développement pour l’avenir.
Pour mémoire, rappelons enfin le principe de fonctionnement des deux modalités d’imagerie qui composent l’imagerie fonctionnelle :
1. La tomographie par émission monophotonique ou TEMP
Elle est réalisée sur une gamma-caméra dont le premier prototype a été mis au point par Hal Anger dès 1957
. Cet appareil est essentiellement constitué d'un collimateur (permettant la sélection angulaire des photons) et de détecteurs de rayons gamma. Amélioré depuis en terme de sensibilité et de rapidité, ce matériel permet de réaliser des scintigraphies
Cet examen consiste à injecter au patient un produit radioactif émettant des rayons gamma. Le choix du produit radiopharmaceutique se fait selon ses capacités à se fixer sélectivement sur l’organe à examiner pour mettre en évidence le fonctionnement de nombreux tissus et organes comme :
- la thyroïde (avec un radionucléide seul comme l’iode 123 (123I),
- le cœur (thalium 201), le cerveau, les reins tous deux avec le technétium 99
- les os avec le marquage au disphosphonate
- les poumons (la ventilation pulmonaire avec un examen de perfusion) (Xénon133)
- et bien d’autres régions anatomiques.
L'image obtenue représente ainsi la distribution du radiopharmaceutique dans la zone examinée.
2.La tomographie par émission de positrons ou TEP
Un examen de TEP vise à faire un bilan du fonctionnement des organes par injection d’un produit de contraste radioactif.
Dans la grande majorité GE Healthcare Discovery MI DR (associant anneau de TEP et scanner) fusionnant TEP et scan sur une même image. des cas, en France, la TEP est utilisée en oncologie pour détecter le cancer, puis pour vérifier l’efficacité de la thérapie anti-cancéreuse.
Dans ce cadre, on injecte au patient un traceur, le fluorodésoxyglucose (FDG) - glucose associé à un radioisotope du fluor, le F18. Dès lors, le principe est le suivant :
• les cellules cancéreuses ont besoin de beaucoup d’énergie pour croître (du glucose),
• le traceur FDG va venir se fixer en priorité sur ces cellules pour les « nourrir »
• le TEP (machine double associant un scanner à rayons X et un anneau de TEP : on parle alors de TEP-Scan) va être capable de détecter et de localiser la suractivité métabolique des cellules cancéreuses.


Le TEP associe deux appareils : un anneau détecteur de TEP et un scanner à rayons X.
Ainsi le TEP que GE a commencé à commercialiser au début des années 90, permet de révéler, ou de confirmer une présence cancéreuse, puis de faire le bilan de l’efficacité des différents traitements (chirurgie, radiothérapie et chimiothérapie). Il constitue un des principaux piliers de l’imagerie oncologique.
Sarah Roy et Guy Lamartine


